Vaksinasi tergesa ala Luhut: Risiko kemahalan dan rasa aman palsu
"Kejar tayang" vaksinasi menuai kritik banyak pihak.
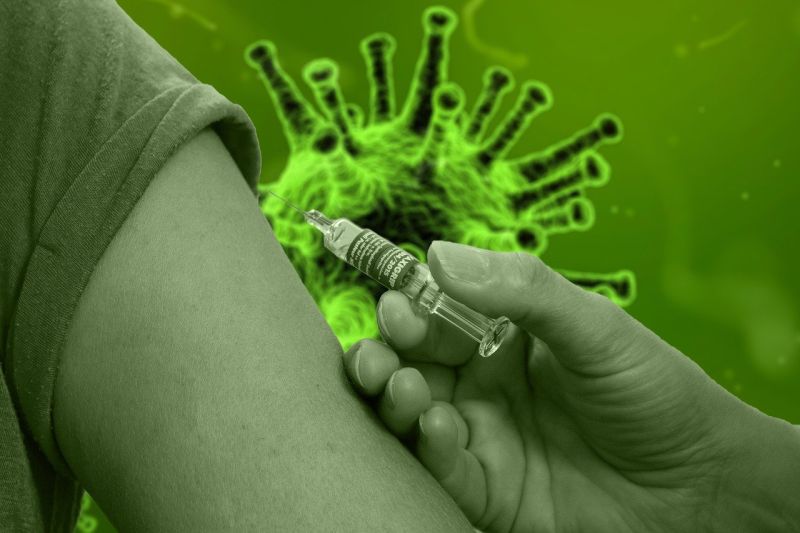
Presiden Joko Widodo mengingatkan jajaran pembantunya untuk menyiapkan rencana pemberian vaksin Covid-19 kepada masyarakat diperhitungkan secara detail dan hati-hati. Kepala Negara tidak ingin vaksinasi melawan virus SARS-Cov itu dilakukan secara tergesa-gesa.
"Semua harus siap, termasuk komunikasi publik mengenai halal dan haram, harga, kualitas, dan distribusinya," cuit Presiden Jokowi melalui akun Twitternya, Senin (19/10).
Rencana pemberian vaksin Covid-19 membutuhkan persiapan yang detail dan hati-hati. Vaksinasi ini tidak akan dilaksanakan secara tergesa-gesa.
Semua harus siap, termasuk komunikasi publik mengenai halal dan haram, harga, kualitas, dan distribusinya. pic.twitter.com/Z9IOWMsB9J — Joko Widodo (@jokowi) October 19, 2020
Presiden tidak menyebut cuitan itu ditujukan kepada siapa. Jika kemudian publik menduga-duga, tentu tak bisa disalahkan. Di jajaran Kabinet Indonesia Maju, salah satu menteri yang getol mendorong percepatan vaksin adalah Menteri Koordinator Bidang Maritim dan Investasi Luhut Binsar Pandjaitan.
Terakhir, Luhut menyinggung percepatan vaksinasi dari tahun 2021 menjadi November di sela kunjungan kerja dan pertemuan bilateral dengan Menteri Luar Negeri China Wang Yi dan jajaran pemerintahan China di Yunan, 11 Oktober lalu. Saat itu Luhut ditemani Menteri Kesehatan Terawan Agus Putranto, Duta Besar RI Djauhari Oratmangun dan Direktur Utama Bio Farma Honesti Basyir.
Pertemuan untuk mengamankan pembelian vaksin Covid-19 yang sudah dirintis Menteri BUMN Erick Thohir dan Menlu Retno Marsudi. Sekaligus persiapan eksekusi vaksinasi, transfer teknologi, dan penjajakan produksi di Indonesia. Selain Wang Yi, hadir jajaran petinggi produsen vaksin Covid-19: Cansino, G42/Sinopharm, dan Sinovac.
Vaksin ketiga perusahaan tengah memasuki tahap akhir uji klinis tahap ketiga. Cansino melakukan uji klinis tahap ketiga di Tiongkok, Arab Saudi, Rusia dan Pakistan. Sedangkan G42/Sinopharm di Tiongkok, Uni Emirat Arab (UEA), Peru, Moroko dan Argentina. Sementara itu, Sinovac melakukan uji klinis tahap ketiga di Tiongkok, Indonesia, Brazil, Turki, Banglades, dan Chile.
Pemerintah China sudah mengizinkan penyuntikan vaksin lewat persetujuan darurat (emergency use authorization), Juli 2020. Pemerintah UAE telah memberikan izin serupa kepada G42/Sinopharm. Indonesia, lewat Badan Pengawas Obat dan Makanan (BPOM), bakal memberi lampu hijau serupa.
Kesanggupan produsen
Masing-masing produsen akan mengirimkan vaksin dalam jumlah berbeda. Pada November ini, Cansino menyanggupi 100.000 vaksin (single dose), dan 15-20 juta pada 2021. G42/Sinopharm menyanggupi 15 juta dosis vaksin (dual dose) tahun ini, 5 juta dosis di antaranya datang pada November depan.
Sinovac menyanggupi 3 juta dosis vaksin hingga akhir Desember 2020. Sinovac berkomitmen mengirim 1,5 juta dosis vaksin (single dose vials) pada minggu pertama November dan 1,5 juta dosis vaksin (single dose vials) lagi pada minggu pertama Desember 2020, plus 15 juta dosis vaksin dalam bentuk bulk.
Untuk tahun 2021, Sinopharm mengusahakan 50 juta (dual dose), Cansino 20 juta (single dose), Sinovac 125 juta (dual dose). Single dose artinya satu orang hanya membutuhkan satu dosis vaksinasi. Sementara dual dose membutuhkan dua kali vaksinasi untuk satu orang.
Untuk memastikan kehalalan vaksin produksi Sinovac dan Cansino, tim inspeksi telah bertandang ke China, 14 Oktober lalu. Tim terdiri dari unsur BPOM, Kementerian Kesehatan, MUI, dan Bio Farma. Sedangkan kehahalan vaksin G42/Sinopharm diambil dari data uji klinis di UAE. "MUI-nya Abu Dhabi sudah menyatakan no issue dengan kehalalan vaksin G42," kata Dirut Bio Farma Honesti Basyir.
Luhut memastikan, China telah memberikan lampu hijau ketiga produsen vaksin Covid-19 berkolaborasi dengan perusahaan Indonesia. Tujuannya, menjadikan Indonesia sebagai produsen penghubung untuk vaksin di Asia Tenggara melalui Bio Farma, BUMN Indonesia yang menjadi salah satu dari 29 produsen vaksin yang telah mengantongi prakualifikasi dari Badan Kesehatan Dunia atau WHO.
China bersedia bekerja sama dengan Indonesia dalam penelitian, produksi dan distribusi vaksin, serta mendukung pertukaran antar lembaga penelitian medis terkait untuk membantu memastikan akses ke vaksin yang terjangkau di seluruh kawasan dan di seluruh dunia," kata Menlu Wang Yi.
"Saya ingin lebih banyak kerja sama antar rumah sakit, pertukaran dokter dan tenaga kesehatan, kolaborasi riset dan teknologi antara kedua negara," menteri Luhut menimpali.
Risiko vaksinasi tergesa
"Kejar tayang" vaksinasi itu menuai kritik banyak pihak. Salah satunya dari epidemiolog Universitas Indonesia, Pandu Riono. Menurut sang "juru wabah", rencana vaksinasi itu tidak layak diteruskan. Bukan saja prosedur pengujian belum rampung, publik juga buta efektivitas dan keandalan vaksin.
"Tidak ada transparansi dalam program vaksinasi, termasuk rencana yangg lengkap, penetapan jenis vaksin, persiapan lapangan, jaminan keamanan, efikasi, biaya dan lain-lain. Bila tidak ada transparansi, maka dapat merugikan, yaitu ketidakpercayaan pada program vaksinasi dasar bagi anak," cuit Pandu.
Lewat Twitternya, @drpriono1, Pandu menegaskan menggelar program vaksin Covid-19 membutuhkan sistem kesehatan publik yang andal. Ia juga mempertanyakan apakah sekarang sudah tersedia vaksin yang benar-benar aman dan efektif.
"(Kita) Tak punya sistem layanan vaksinasi orang dewasa, sangat beda dengan (layanan) vaksinasi anak balita. Belum ada sistem monitoring dan evaluasi. Tak ada transparansi pada publik dan ahli. Kenapa buru-buru?" cuit dia, diambil Alinea.id, Selasa (20/10).
Menggelar program vaksin Covid-19 butuh sistem kesehatan publik yg andal. Adakah Vaksin yg benar2 AMAN & Efektif? Tak punya sistem layanan vaksinasi orang dewasa, sangat beda dg vaksinasi anak balita. Belum ada Sistem Monev. Tak ada Transparansi pada publik & Ahli. Kenapa buru2? — Juru Wabah (@drpriono1) October 18, 2020
Rencana vaksinasi secara besar-besaran pada November atau Desember juga dipertanyakan Yohanes Cakrapradipta Wibowo, kandidat PhD Experimental Pharmacology di University of Heidelberg, Jerman.
Menurut dia, dari ketiga jenis vaksin itu belum ada yang dinyatakan aman dan ampuh untuk mendongkrak imunitas masyarakat karena belum lolos uji klinis tahap ketiga. Ini tahap terakhir uji klinis pada manusia sebelum vaksin diproduksi massal. Ketiga vaksin masih dalam tahap uji klinis tahap akhir.
Uji klinik kandidat vaksin
Saat ini ada sekitar delapan kandidat vaksin yang memasuki uji klinis tahap tiga. Menurut WHO, hasil uji klinis paling cepat diketahui pada Desember atau awal tahun depan. Itu pun baru laporan awal apakah apakah vaksin aman dan ampuh atau tidak. Belum termasuk proses produksi dan distribusinya.
WHO, kata dia, memperkirakan vaksin yang lolos uji tahap akhir baru akan tersedia pada pertengahan tahun depan. Dari informasi yang dia telisik, Yohanes menjelaskan, laporan hasil uji klinis tahap ketiga vaksin produksi Sinovac oleh Universitas Padjajaran paling awal baru didapat Januari 2021. Itu pun baru petunjuk indikasi hasil positif atau tidak. Uji klinis baru usai pada September 2020.
Vaksin G42 yang dikembangkan oleh China dan Uni Emirat Arab (UEA), rilis laporan riset hasil uji klinis vaksin dengan partisipan 45.000 orang ini paling cepat muncul Maret 2021. "Uji klinis bisa berhasil atau sebaliknya. Riset ini juga diperkirakan selesai pada September tahun depan," jelas Yohanes.
Terakhir, vaksin Cansino yang sedang dilakukan uji klinis fase ketiga kepada 40.000 partisipan. Laporan riset paling awal akan rilis pada Desember 2021 dan uji klinik diperkirakan selesai pada Januari 2022.
"Tidak semua uji klinik tahap tiga berjalan mulus. Tidak semua vaksin dalam setiap fase (ada 4 fase) akan berjalan mulus karena proses yang dilakukan saat ini adalah proses percepatan walau tidak mengabaikan setiap fase yang perlu dilakukan. Karena darurat, ada penyederhanaan proses dari yang seharusnya."
Tolak 'vaksin setengah jadi'
Keputusan terburu-buru itu mendorong Yohanes membuat petisi menolak 'vaksin setengah jadi' di laman Change.org. Dokter dan peneliti yang berkecimpung dalam riset kedokteran itu menuliskan petisi pada Minggu (18/10) lalu. Per Senin (19/10) pukul 21.00 WIB, petisi telah diteken 346 orang.
Penolakan selain didasari belum ada vaksin yang lolos uji klinis fase ketiga, juga belum ada lembaga otoritas seperti WHO yang merekomendasikan penggunaan vaksin-vaksin tersebut. Menurut dia, dalih persetujuan darurat berpotensi menimbulan masalah. Karena itu, tidak boleh dijadikan legitimasi mutlak.
"Apalagi persetujuan darurat yang dikeluarkan oleh negara lain tanpa ada analisis data dan pertimbangan yang matang," tulis dia.
Ia mencontohkan di Amerika Serikat saat persetujuan darurat untuk obat Hidroksiklorokuin yang dipromosikan oleh Presiden Donald Trump tiba-tiba diterbitkan oleh Food and Drug Administration (FDA) tanpa ada penjelasan ilmiah yang logis. Akhirnya, bukti riset terbaru (solidarity trial) menunjukkan obat ini tidak bermanfaat.
"Vaksin 'setengah jadi' ini berpotensi menimbulkan masalah baru jika timbul efek yang tidak diinginkan. Apalagi tenaga medis menjadi salah satu prioritas pemberian vaksin. Padahal, sektor kesehatan sudah terpukul hebat saat pandemi ini," tulis Yohanes.
Pemerintah, kata Yohanes, diminta tidak latah dan membuat masyarakat terjebak dengan rasa aman palsu. Dia mengingatkan, salah satu elemen penting dalam pembuatan vaksin adalah seberapa aman dalam meningkatkan kekebalan tubuh. Juga seberapa lama dampak imunitas vaksin bisa bertahan.
Apabila vaksin yang sudah siap itu daya lindungnya rendah, kata dia, akan membutuhkan lebih banyak dosis vaksin. Ini bakal membuat biaya membengkak.
"Itu artinya para pengguna vaksin bisa terjebak dalam rasa aman palsu. Ini justru berbahaya karena berpotensi menyebarkan virus corona lebih luas."
Jaminan Menkes Terawan
Sebagai pelaksana vaksinasi, Menteri Terawan Agus Putranto menjamin penyuntikkan akan berlangsung kredibel. Ia menguraikan, persiapan detail vaksinasi masih terus dilakukan. Sejak akhir September 2020, kata dia, telah dilaksanakan pelatihan kepada tenaga kesehatan mengenai tata cara vaksinasi Covid-19.
Terawan menjelaskan, prioritas vaksinasi diberikan kepada para tenaga kesehatan dan aparat keamanan yang berada di garis terdepan dalam penanganan Covid-19.
"Pada tahap awal, kami akan memberikan prioritas vaksin kepada mereka yang di garda terdepan, yaitu medis dan paramedik, pelayanan publik, TNI/Polri, dan seluruh tenaga pendidik," kata Terawan, disitat dari maritim.go.id, Selasa (20/10).
Untuk memastikan kesiapan fasilitas kesehatan di Indonesia , kata Terawan, pihaknya segera melakukan simulasi di beberapa puskesmas sasaran. Untuk menjaga akuntabilitas pengadaan vaksin, kata dia, vaksin yang dibayarkan pemerintah maupun yang mandiri tetap harus melalui Bio Farma, sebagai BUMN yang ditunjuk untuk pengadaan vaksin.
Sebagai bagian dari transparansi dan akuntabilitas, jelas Terawan, dalam waktu dekat Bio Farma diminta memaparkan kepada publik mengenai biaya pembelian vaksin dari semua mitra kerjasamanya.
Selain yang berada di garda terdepan penanganan Covid-19, mereka yang tidak mampu secara ekonomi biaya vaksinasinya akan ditanggung pemerintah. "Mereka yang di garda terdepan dan peserta Penerima Bantuan Iuran alias PBI dalam BPJS Kesehatan akan ditanggung biaya vaksinnya oleh Pemerintah."

Derita jelata, tercekik harga pangan yang naik
Senin, 21 Feb 2022 17:25 WIB
Menutup lubang “tikus-tikus” korupsi infrastruktur kepala daerah
Minggu, 13 Feb 2022 15:06 WIB
Segudang persoalan di balik "ugal-ugalan" RUU IKN
Minggu, 23 Jan 2022 17:07 WIB
Ironi hilirisasi: Glorifikasi di balik nestapa masyarakat
Selasa, 23 Jan 2024 18:50 WIB
Mewujudkan e-commerce inklusif bagi penyandang disabilitas
Kamis, 30 Nov 2023 16:09 WIB